Серебро. Химический элемент, символ Ag (лат. Argentum, от лат. – светлый, белый, англ. Silver, франц. Argent, нем. Silber). Имеет порядковый номер 47, атомный вес 107, 8, валентность I. II, плотность 10, 5 г/см3, температура плавления 960, 5°С, кипения 2210°С.
Серебро – металл белого цвета, практически не изменяющийся под воздействием кислорода воздуха при комнатной температуре, однако из-за наличия в воздухе сероводорода со временем покрывается тёмным налётом сульфида серебра Ag2S:
4Ag + O2 + 2H2S = 2Ag2S + 2H2O.
Удалить этот сульфид с поверхности серебряного изделия можно механически, используя различные чистящие пасты или тонкий зубной порошок.
Серебро устойчиво в воде, соляная, разбавленная серная кислота и царская водка на него не действуют, поскольку на поверхности металла образуется защитная плёнка его хлорида AgCl. Серебро растворяется в азотной кислоте:
Ag + 2HNO3 = AgNO3 + NO2 + H2O.
Как и золото, серебро взаимодействует со щелочными растворами цианидов.
При добавлении к раствору нитрата серебра щёлочи выделяется тёмно-коричневый осадок оксида серебра:
2AgNO3 + 2NaOH = 2NaNO3 + Ag2O + H2O.

Серебро хорошо полируется, имеет высокую (95%) отражательную способность (лучшие зеркала делают с использованием серебра); оно обладает хорошей ковкостью (уступает только золоту) и самой высокой из всех металлов тепло- и электропроводностью. Чтобы повысить твёрдость и прочность серебра, его используют в сплавах с другими металлами.
Серебро хорошо паяется мягкими припоями, используется как основа группы твёрдых припоев, для предварительного серебрения радиодеталей перед пайкой, в контактах реле, в разъёмах, для чеканки монет, изготовления ювелирных изделий, столовых приборов, медицинских инструментов, производства серебряно-цинковых аккумуляторов, для кинофотоматериалов и т.д. Для особо ответственных приборов чистое серебро служит материалом предохранителей.
Серебро для конструкционных целей используют обычно в виде сплавов. Его применяют также в качестве легирующего элемента и для нанесения защитных антикоррозийных покрытий.
Ионы серебра обладают хорошими антисептическими свойствами и уже в незначительной концентрации стерилизуют питьевую воду, убивая микроорганизмы. Ещё древние египтяне клали на открытые раны серебряные пластинки: тогда рана не загнивала и быстро заживала.
Серебро является постоянным спутником золота и часто находится в нём в виде примеси.
Основные физические и механические свойства серебра:
Атомная масса ……………………………………………………107, 87
Плотность, г/см3 ……………..……………………………………10, 49
Температура, °С:
плавления ……………………………………………960, 5
кипения ……………………………………………… 2210
Скрытая теплота плавления, кал/г………………………….. 25
Удельная теплоёмкость, кал/ (г . град) …………………….. 0, 056
Удельное электросопротивление, мкОм . см ………………1, 62
Теплопроводность, кал/ (см . сек . град)…………………………….0, 974
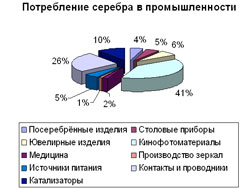
Основные ниши использования серебра: по серебрение изделий, ювелирные изделия, медицина, источники питания, катализаторы, столовые приборы, кинофотоматериалы, производство зеркал, электронные компоненты.

Оставить комментарий